JCI:揭示患者疾病缓解后乳腺癌细胞在机体骨髓中得以存活背后的分子机制
发布时间:2024-12-16 字号:【 大 中 小 】
雌激素受体阳性的乳腺癌是乳腺癌最常见的一种形式,当患者疾病缓解后,这类癌细胞往往能在骨髓中存活数年甚至数十年,这些细胞在骨髓中的持续存在会导致大约40%的患者发生乳腺癌复发。而这种复发或会表现为侵袭性的骨癌,并会伴有骨折和高钙血症等疾病症状,这些细胞还会扩散到机体其它器官中并引起无法治愈的复发性疾病。
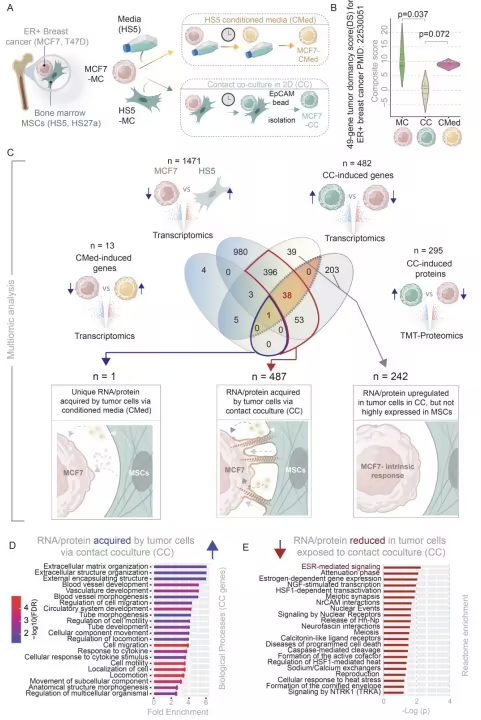
多组学分析揭示接触共培养中ER+乳腺癌细胞从间充质干细胞中获得的RNA/蛋白
为了能更好地理解这些细胞存活背后的分子机制,以及为何其会导致如此严重的复发性疾病,研究人员调查了骨髓中这些分散细胞到底会发生什么?文章中,他们揭示了骨髓中的间充质干细胞支持癌细胞生长背后的分子机制。医学博士Gary Luker说道,我们发现,乳腺癌细胞需要直接与间充质干细胞相互接触,这些癌细胞会直接从间充质干细胞中借用诸如蛋白质和信使RNA分子等分子,从本质上来讲,间充质干细胞就好比是非常慷慨的邻居,其能提供物质并让癌细胞变得更具侵袭性和药物耐受性。
在实验室中,癌细胞和间充质干细胞之间的接触就会导致数百种蛋白质发生改变,进一步分析到底是哪些蛋白质能促使乳腺癌细胞存活,让研究人员将目光集中到了名为GIV(也称之为Girdin)的分子上,研究者指出,GIV能驱动多种癌症出现侵袭性、化疗耐受性、获得转移性潜能等;GIV还会促使癌细胞对雌激素靶向性疗法(尤其是药物他莫昔芬)变得更具耐受性,研究人员希望对癌细胞存活背后机制的理解或在未来有望帮助开发预防雌激素受体阳性的乳腺癌复发的新型疗法。
Pradipta Ghosh教授说道,休眠的细胞能被重新唤醒并引起雌激素受体阳性的乳腺癌在多年后复发(在某些情况下长达十年时间),而这往往发生于患者被认为处于疾病缓解期之后。由于这些癌细胞能通过细胞通道从骨髓中的干细胞借用必需的蛋白质,这就好像走私一样,而靶向左右其所“走私”的通道或蛋白质的方法或能帮助预防雌激素受体阳性的乳腺癌的复发和转移。综上,本文研究结果提供了关于间充质干细胞到肿瘤细胞之间进行胞间运输的多组学见解,并验证了GIV分子的运输如何调节雌激素受体阳性乳腺癌疾病状态。(生物谷Bioon.com)
文章来源:生物谷
官网链接:https://www.bioon.com/
微信公众号二维码:
